(一)行业主要法律法规及政策
参考观研天下发布《2018年中国体外诊断行业分析报告-市场运营态势与投资前景研究》
1、行业主要法律法规
体外诊断行业在我国的医疗器械监管政策领域经历了几个历史发展时期,按照国际对医疗器械的定义,体外诊断试剂属于医疗器械,但有其特殊性,产品介于药品和普遍意义上的医疗器械之间,简单的按药品或器械管理都不甚合理。根据国际各个国家的法律,将体外诊断试剂划归器械并增加专用要求是国际通行的做法。欧盟和美国FDA 均将体外诊断试剂划归医疗器械进行管理,日本单独将体外诊断试剂列为一类,与药品、医疗器械平行管理。我国监管体系不断完善,体外诊断试剂产品的监管也经历了一系列重大的变化,直至2007 年一系列针对体外诊断试剂监管的法规出台,明确了按照医疗器械的监管范围和要求。

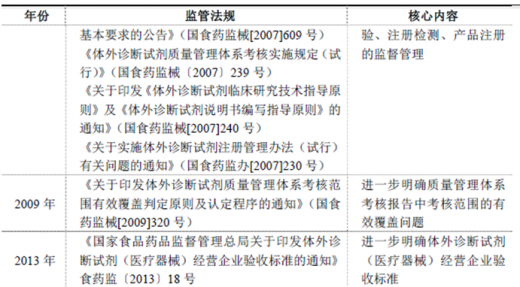



2、行业主要政策
(1)诊断领域产业化启动
2005 年12 月,国家发改委发布《国家发展改革委办公厅关于组织实施生物疫苗和诊断试剂高技术产业化专项的通知》,从而在政策上启动了诊断技术的产业化。该通知主要内容是通过实施生物疫苗和诊断试剂高技术产业化专项,提高我国生物医药产业技术创新能力和国际竞争力,提高广大人民群众的医疗健康水平,推动我国生物医药产业的持续、快速、健康发展,重点发展预防性疫苗、治疗性疫苗和诊断试剂。其中诊断试剂以免疫诊断、分子诊断等新型检测试剂为重点,开展酶联免疫检测法(ELISA)、胶体金、免疫荧光、多聚酶链反应法(PCR)等新型诊断试剂和智能化诊断系统的技术开发和产业化。
(2)政策扶植产业科技研究、加速产业发展
《国家中长期科学和技术发展规划纲要(2006-2020)》中明确研制重大新药和先进医疗设备作为规划目标。攻克新药、大型医疗器械、医用材料和释药系统创制关键技术,加快建立并完善国家医药创制技术平台,推进重大新药和医疗器械的自主创新。
《国家“十一五”科学技术发展规划》以及《国家“十二五”科学技术发展规划》中均提出艾滋病和病毒性肝炎等重大传染病防治。突破检测诊断、监测预警、疫苗研发和临床救治等关键技术,新型疫苗与治疗药物创制等关键技术,自主研制高效特异性诊断试剂,提升重大传染病的应急和综合防控能力,有效降低艾滋病、病毒性肝炎、结核病的新发感染率和病死率。
“十二五”期间,体外诊断技术纳入《“十二五”生物技术发展规划》,“体外诊断技术产品开发”列为“十二五”863 计划生物和医药技术领域的重大项目。国家高技术研究发展计划(863 计划)扶植体外诊断产业发展,设立了“体外诊断技术产品开发”重大项目,总体目标是突破一批体外诊断仪器设备与试剂的重大关键技术,研制出一批具有自主知识产权的创新产品和具有核心竞争力的产品,在一体化化学发光免疫诊断系统等高端产品方面实现重点突破。其中一个重点课题是《开放式全自动管式化学发光免疫检测系统的研制》,目标是实现开放式全自动管式化学发光免疫检测仪器及配套试剂的一体化检测,突破关键技术。
《“十三五”国家科技创新规划》将艾滋病和病毒性肝炎等重大传染病防治列入国家科技重大专项项目之一,要求突破突发急性传染病综合防控技术,提升应急处置技术能力;攻克艾滋病、乙肝、肺结核诊防治关键技术和产品,加强疫苗研究,研发一批先进检测诊断产品,提高艾滋病、乙肝、肺结核临床治疗方案有效性,形成中医药特色治疗方案。关于体外诊断产品,需突破微流控芯片、单分子检测、自动化核酸检测等关键技术,开发全自动核酸检测系统、高通量液相悬浮芯片、医用生物质谱仪、快速病理诊断系统等重大产品,研发一批重大疾病早期诊断和精确治疗诊断试剂以及适合基层医疗机构的高精度诊断产品,提升我国体外诊断产业竞争力。
《“十三五”生物产业发展规划》要求推动重点生物医药领域新发展,包括提供快速准确便捷的检测手段。针对急性细菌感染、病毒感染等重大传染性疾病,包括外来重大传染性疾病的检测需求,加速现场快速检测的体外诊断仪器、试剂和试纸的研发和产业化。针对糖尿病、高尿酸血症、高脂血症等慢性病,加快便捷和准确的家用体外诊断产品的产业化。加快特异性高的分子诊断、生物芯片等新技术发展,支撑肿瘤、遗传疾病、罕见病等疾病的体外快速准确诊断筛查。完善产业链的配套建设,发展配套的高精度的检测仪器、试剂和智能诊断技术,支持第三方检测中心发展与建设。
(3)战略性产业发展规划
2009 年6 月,国务院印发《促进生物产业加快发展若干政策通知》,提出加快培育生物产业,加快把生物产业培育成为高技术领域的支柱产业和国家的战略性新兴产业。加快发展生物医学材料、临床诊断治疗康复设备等。
2010 年4 月,国家人口计生委财政部关于开展国家免费孕前优生健康检查项目试点工作的通知:为降低出生缺陷发生风险,提高出生人口素质,根据《中华人民共和国人口与计划生育法》和《中共中央国务院关于全面加强人口和计划生育工作统筹解决人口问题的决定》,经国务院批准,国家人口计生委、财政部共同组织实施国家免费孕前优生健康检查项目试点工作。
2012 年1 月,科技部发布《医疗器械科技产业“十二五”专项规划》,提出到2015 年,初步建立医疗器械研发创新链,医疗器械产业技术创新能力显著提升;突破一批共性关键技术和核心部件,重点开发一批具有自主知识产权的、高性能、高品质、低成本和主要依赖进口的基本医疗器械产品,满足我国基层医疗卫生体系建设需要和临床常规诊疗需求。其中重点支持的项目包括高性能免疫分析系统、核心部件及新型诊断试剂以及现场快速检测仪器(POCT),打破进口垄断,降低医疗费用,提高产业竞争力。
2012 年5 月,国务院讨论通过了《“十二五”国家战略性新兴产业发展规划》,其中将生物产业作为重点发展的七大产业之一,加快先进医疗设备、医用材料等生物医学工程产品的研发和产业化,促进规模化发展。重点支持包括创新药物、现代中药、医疗器械和生物医学工程等,上述领域未来将获得更多的税收优惠、政府扶持基金和技术支持。
2012 年5 月,卫生部发布的《中国慢性病防治工作规划(2012-2015 年)》提出,各级各类医疗机构对35 岁以上人群实行首诊测血压制度。80%以上的乡镇卫生院开展血糖测定,30%以上的乡镇卫生院开展简易肺功能测定,40%的社区卫生服务中心和20%的乡镇卫生院开展口腔预防保健服务。开发癌症高发地区重点癌症筛查适宜技术,开展早期筛查和治疗。
2012 年10 月,国务院发布的《卫生事业发展“十二五”规划》中提到至2015年,血液筛查核酸检测基本覆盖全国。做好以宫颈癌和乳腺癌筛查为重点的农村常见妇女病防治工作,2015 年农村适龄应检妇女常见病检查率达到70%。加大出生缺陷干预力度,开展出生缺陷三级综合防治,加强婚前孕前保健宣传教育、产前筛查和产前诊断、新生儿疾病筛查管理,降低严重多发致残的出生缺陷发生率。到2015 年,新生儿遗传代谢性疾病筛查覆盖率达到70%。
2012 年12 月,国务院发布《生物产业发展规划》,提出“大力发展新型体外诊断产品。围绕早期筛查、临床诊断、疗效评价、治疗预后、出生缺陷诊断等需求,开发高通量、高精度的体外诊断仪器、试剂和体外诊断系统。加快发展分子诊断、生物芯片等新兴技术,加速免疫、生物标志物、个体化医疗、病原体等体外诊断产品的产业化;发展可现场快速检测的血液、生化、免疫、病原体等体外诊断仪器及试剂的制备技术,促进规模化生产。建设体外诊断试剂研发和产业化平台,加强原料酶、诊断性抗体等试剂原料基地建设,构建量值溯源体系及其参考实验室网络,推动我国体外诊断产业的发展。”2013 年2 月16 日,国家发改委发布的《产业结构调整指导目录(2011 年本)(2013 年修订)》提出将“新型诊断试剂的开发和生产”、“新型医用诊断医疗仪器设备”列为第十三大类“医药”中的鼓励类项目。
2013 年2 月28 日,国家发改委、财政部、工业和信息化部、卫生部等部门联合发文《关于组织实施2013 年高性能医学诊疗设备专项的通知》,该通知要求:为了满足我国人民群众重大疾病诊疗需求,专项拟聚焦市场需求紧迫、应用面广、引领带动作用强的医学诊疗设备领域,通过需求侧和供给侧双向激励,促进一批高性能新产品产业化及示范应用,培育壮大一批研发能力强、具有自主知识产权的优势企业,带动全产业链协调发展,构建比较科学合理的研发、产业化、示范应用体系,大幅提升产业内生发展能力。
2013 年9 月28 日,国务院发布的《国务院关于促进健康服务业发展的若干意见》指出到2020 年,基本建立覆盖全生命周期、内涵丰富、结构合理的健康服务业体系,打造一批知名品牌和良性循环的健康服务产业集群。健康服务业总规模达到8 万亿元以上,成为推动经济社会持续发展的重要力量。
2014 年6 月5 日,国家卫计委下发的《关于控制公立医院规模过快扩张的紧急通知》指出将引导医疗机构合理配置,逐步提高国产医用设备配置水平,加快体外诊断领域的进口替代进程。随后,国家卫生计生委、工业和信息化部8月16 日在京联合召开推进国产医疗设备发展应用会议,会议提出要大力倡导卫生计生机构使用国产医疗设备,重点推动三级甲等医院应用国产医疗设备,促进健康服务业发展。
2015 年2 月16 日,科技部发布《关于开展科技部“十三五”国家重点研发计划优先启动重点研发任务建议征集工作的通知》,提出将体外诊断纳入科技部关于开展“十三五”国家重点研发项目征集范围。
2016 年11 月29 日,国务院发布“十三五”国家战略性新兴产业发展规划,提出开发高性能医疗设备与核心部件从而提升生物医学工程发展水平,包括加速发展体外诊断仪器、设备、试剂等新产品,推动高特异性分子诊断、生物芯片等新技术发展,支撑肿瘤、遗传疾病及罕见病等体外快速准确诊断筛查。同时,发展专业化诊疗机构,培育符合规范的液体活检、基因诊断等新型技术诊疗服务机构以增强生物技术对消费者的专业化服务能力。
2017 年1 月10 日,国务院在《“十三五”卫生与健康规划的通知》中列出的主要任务指出,要加快健康产业发展,大力发展社会办医,创新发展药品、医疗器械等产业。鼓励创新药和临床急需品种上市。支持企业兼并重组、强强联合,培育具有国际竞争力的大型企业,提高产业集中度。支持提升医疗设备的产业化能力和质量水平,推进发展应用。
2017 年5 月23 日,国务院办公厅印发《关于支持社会力量提供多层次多样化医疗服务的意见》,鼓励社会力量提供医疗服务,有序发展前沿医疗服务。鼓励有实力的社会办医疗机构瞄准医学前沿,组建优势学科团队,提供以先进医疗技术为特色的医疗服务。推动经依法依规批准的新型个体化生物治疗产品标准化规范化应用。推广应用高性能医疗器械。持续推动成熟可靠的前沿医疗技术进入临床应用的转化机制建设。
(4)主要进口国家及地区相关政策
公司产品出口主要集中在亚洲、欧美等国家或地区。这些国家或地区绝大多数已与我国签有互利贸易协定或者加入世界贸易组织,在相关贸易协定的框架下除需要求相关认证(如ISO9001、ISO13485、欧盟CE 认证、美国FDA 认证等)及注册外,进口国政府对公司出口的产品无特殊贸易限制,进口政策相对宽松,与我国很少发生贸易摩擦。同时按国际惯例,中国食品药品监督管理机关代表中国政府对境内企业生产的医疗器械产品进行产品安全性和合法性审查,核发出口销售证明,证明该产品准许出口销售。
|
主要进口国家及地区相关政策 |
|
|
欧盟 |
欧盟于2012 年6 月1 日起开始正式实施IEC60601-1 第三版,出口至欧盟的医疗器械也已开始遵照第三版要求。第三版在技术要求、安全理念等方面有较大改变,要求也更多、更复杂,势必延长了医疗器械产品的检测和注册时间,从而延长产品上市时间,增加产品的注册成本。另外,转化及实施IEC60601-1第三版标准也会极大地影响到医疗器械生产企业的产品设计,研发和生产规划。针对出口欧盟标准的提高,国内医疗器械企业需全面而深入地研究IEC60601-1 第三版标准,才能有利于保持与国际先进标准的一致性,进而保障医疗器械产品安全有效、拓展欧盟市场,促进医疗器械产业的发展。 另外,新的WEEE(报废电子电器设备)指令2012/19/EU 也已于2012 年8月13 日生效,我国医疗器械出口欧盟也面对新的环保壁垒。新WEEE 指令还规定了适用的电气电子设备范围。从2012 年8 月13 日~2018 年8 月14 日为过渡期,在这一时期内新指令适用的医疗器械包括了放射治疗设备、心血管相关的设备、透析设备、肺部通气机、核医学设备、体外诊断用实验设备、分析仪、冷冻仪、授精测试仪器以及其他用于检测、预防、监控、治疗、缓解疾病伤痛或残疾的器具等,但不包括植入型的以及可感染的产品。从2012 年8 月15 日开始,新指令将涵盖所有外部直径大于50cm 的大型医疗器械以及所有外部直径小于50cm 的小型医疗器械,但不包括在使用寿命结束之前可能具有感染性、引起潜在感染的医疗器械、体外诊断医疗器械。 |
|
美国 |
美国食品和药物管理局(Food and
Drug Administration 简称FDA),FDA通过实施《联邦食品、药品和化妆品法》、《公平包装和标识法》、《公众健康服务法》、《医疗器械安全性法规》、《医疗器械修正案》等法律法规确保医疗器械等产品的安全有效,其对进口医疗设备也同样适用。 在税收方面,美国新实施的《国内税收法》开始征收医疗设备消费税,指出2012 年12 月31 日以后出售的所有供人类使用的医疗设备(包括牙医用具、牙医设备、体外诊断试剂及仅供研究使用的设备)都必须缴付2.3%的消费税。 |
|
东盟 |
医用敷料和诊疗设备是我国对东盟出口的两类主要产品。根据中国-东盟自由贸易区相关协议,零关税和各项贸易的便利化政策,加上双边地缘比邻的优势,东盟对我国的相关进口政策将有助于医疗设备出口的持续增长。 |
(二)我国体外诊断行业经营模式与利润水平
1、行业特有的经营模式
(1)销售模式
目前我国体外诊断企业销售模式分为厂家直销和渠道经销商销售两种,经销商模式是行业的主要销售模式。经销商一般具有地区性,在区域内具有良好的医院资源和客户关系,可以协助企业快速构建全国范围内的营销网络。
(2)定价模式
目前国内体外诊断产品定价普遍实行招投标模式,与国家对药品价格的严格指导控制方式不同。在定价招投标模式下,各地区医疗卫生机构一般委托独立第三方对年度拟采购的诊断产品进行招标,只有投标价不高于采购预算价且质量合格的厂商才能中标。
(3)售后服务及配套模式
国内体外诊断企业一般直接提供技术支持及售后服务。在售后服务方面,国内企业具备突出的快速响应优势;同时,很多企业经过培养和协助,支持渠道经销商自主进行售后服务。
2、行业利润水平及其变动趋势
体外诊断行业属于高新技术产业,行业利润水平较高,国内企业综合毛利率一般在50%以上,行业总体利润水平保持相对平稳。

国内体外诊断行业受益于医疗市场的快速增长,预计“十三五”期间,在整体物价及劳动力成本可控状态下,行业总体毛利率水平继续保持平稳状态。未来几年体外诊断的市场需求稳步增长,受经济影响不大,利润增长可持续性较强;体外诊断新产品研发和创新对利润的贡献份额大,经济附加值高。
目前我国体外诊断领域生产企业规模普遍较小,掌握关键核心技术的企业不多,产品竞争力不强,未来可能面临竞争加剧、产品降价的风险,一定程度上影响行业利润率水平。
(三)行业的周期性、区域性和季节性特征
1、周期性
体外诊断行业属于弱周期性行业。其下游行业与生命健康关系密切,需求与本地区经济及医疗水平相关,需求刚性较强,因此行业周期性特征不明显,波动较低,行业抗风险能力较强。
2、区域性
体外诊断产品下游市场主要为医院临床检验、体检中心、医学独立实验室等,市场需求与医疗事业发展和医疗保健支出水平联系紧密,由此形成各国家及国内各地区之间的区域性差异。
在体外诊断的全球市场上,北美、欧洲、日本合计占据70%的市场份额。
金砖四国基础弱,但是近年来增长最快的市场,尤其是中国体外诊断市场发展迅猛。
受区域经济发展水平影响,体外诊断行业消费需求呈现地域特征,市场需求主要集中在人口密集、经济发达的地区以及医疗服务水平较高的各省一二线城市,长三角、珠三角和环渤海经济区市场需求较为突出。
3、季节性
受下游需求市场的影响,行业存在一定的季节性销售特征。国内一季度节假日较多,就诊、体检的人数较少,体外诊断试剂需求相对较小;四季度由于季节变化明显,疾病发病率较高,就诊、体检的人数增多,体外诊断试剂的需求最大。而体外诊断仪器国内销售的季节性则不太明显。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。