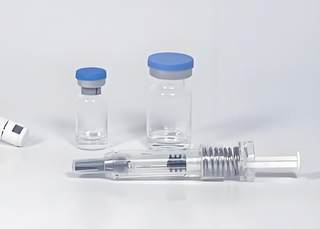
根据我们创新药周期理论,1970年-1990年是全球创新药的研发突破期,本章我们将回顾日本药企如何在1980年代把握住这波周期,快速做强做大。
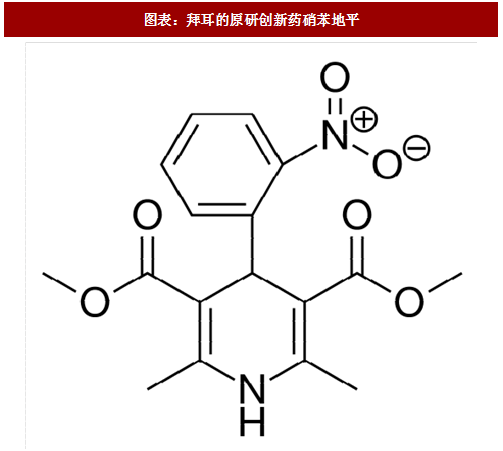
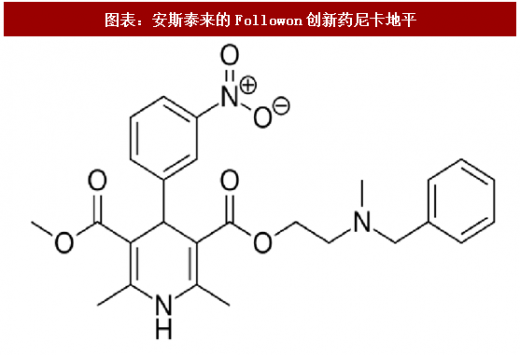
与尚未改革开放的中国不同,日本现代制药工业在上世纪70年代以仿制药起步,龙头药企恰好赶上了80年代创新药的研发突破期,从而缩小了与欧美药企研发领域的差距。由于彼时日本药企自身研发基础仍然薄弱,难以实现首创新药(First-in-class)的突破,所以大部分药企采取跟随式创新(Follow-on)的策略。下面的例子是拜耳原研的硝苯地平以及日本80年代上市的“创新药”尼卡地平,可以看出二者左侧化学结构完全相同,按照第一三共的说法尼卡地平右侧官能团可以增加选择性以及延长半衰期。
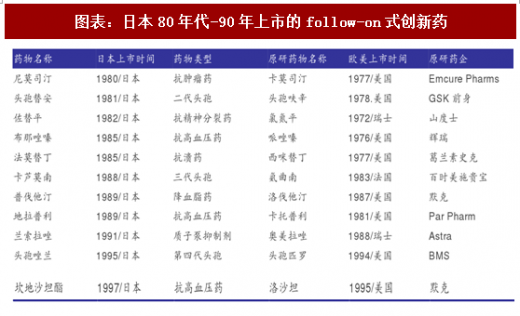
欧美70年代开始的研发爆发期,给日本制药工业带来了千载难逢的机遇,坐享了欧美50年代-70年代十几年的基础理论红利,节省了时间、经济成本。欧美重磅创新药物上市之后,日本药企往往在几年之内就能上市同一靶点的跟随式创新药物,伴随日本药企自身技术的积累,这种时差有逐步缩小的趋势,从80年代的5年左右到90年代已经下降到2年左右,不仅如此,90年之后上市的兰索拉唑、坎地沙坦酯等创新药在副作用等方面较原研药品有相对优势,完成了从me-too向me-better药物的转型。
虽然日本制药行业在创新药领域自80年代开始取得了长足的进步,但是由于药品上市与达到销售峰值存在滞后效应,80年代日本医药市场的畅销药品还比较少见到这批创新药的身影,反而仍然是日本版本的“神药”大行其道,一个例子:云芝多糖K(Krestin),是一种从多孔菌科植物提取的高分子糖肽聚合物,具有化学惰性,对人体几乎没有作用。
在美国和欧洲等发达国家,云芝多糖K由于缺乏有效性,未能获得监管部门的批准。然而在日本,该产品由于绝对的安全性成功上市,临床应用于抗肿瘤,1986年成为日本畅销药冠军,销售额高达2.96亿美元,占当时肿瘤药市场规模的7%。而同样是1986年,GSK的创新药雷尼替丁成为历史上首个销售额超过10亿美元的重磅炸弹药物。
我们认为日本80年代创新药的萌芽与我国2008年到2017年的状态很类似,虽然部分走在前面的药企以me-too类创新为突破口,已经开始了多年的研发积累,但是市场仍以中药注射剂等特色处方药为主。
日本90年代之后,创新药逐渐凭借治疗效果完成对“神药”的替代,清流第一次成为主流。彼时的日本人口结构老龄化、医保控费等背景与此时的我国非常相似,市场上有很多关于这方面的研究这里不再做展开,形似日本而走中国自己的特色是我们对未来的判断,具体分析在1.5部分。
二、创新药周期理论的应用之二:创新药的衰退期是仿制药崛起的黄金期
根据我们的创新药周期理论,2000年之后专利药保护陆续到期,进入上一轮创新药周期的衰退阶段,然而“彼之毒药我之蜜糖”,创新药的衰退期恰恰是仿制发展的黄金期。市场曾经认为中国仿制药制剂出口与印度仿制药相差了15年,然而制剂出口的大逻辑至今已经有十几年,中国仍然没有出现真正能与海外仿制药分庭抗礼的竞争对手。根据我们提出的创新药周期理论,我们认为我国与国际仿制药巨头不仅仅是相差了15年,而是错过了2000-2010年的窗口期。本章节我们将回顾国际仿制药市场发展历史,用我们提出的创新药周期理论解释为何我国仿制药企业没能赶上国际竞争对手。
1、1Hatch-Waxman法案的颁布是一切的开始
1984年,美国通过《药品价格竞争与专利期补偿法》(又名:Hatch-Waxman法案),该法案有利于仿制药企业,有利于医保支付机构,不利于原研药企业。Hatch-Waxman法案颁布前的1983年,只有35%的品牌药在专利过期之后有仿制药竞争对手上市,仿制药处方量只占总处方量的13%,而2016年仿制药处方量占总处方比值已达86%。可以说没有Hatch-Waxman就没有美国仿制药市场。
在Hatch-Waxman法案之前,美国几乎不存在仿制药市场,因为品牌药深入人心,即使品牌药专利过期之后仍然保持畅销。仿制药企业需要在专利药过期之后,重复再做一遍临床前实验、临床试验,资金、时间成本惊人。
Hatch-Waxman法案通过后,仿制药申请人仅需向FDA提供数据证明该仿制药药学等效且生物等效即可,不再需要开展大规模的临床试验。Hatch-Waxman法案等于宣布了通用名药物只要化学结构与原研相同,制剂工艺与原研接近,则疗效一定等效,这大大的降低了仿制药门槛,打消了患者对通用名药物的疑虑。自法案颁布后,FDA接受的ANDA数量逐年增长,越来越多的专利受到了仿制药的挑战。
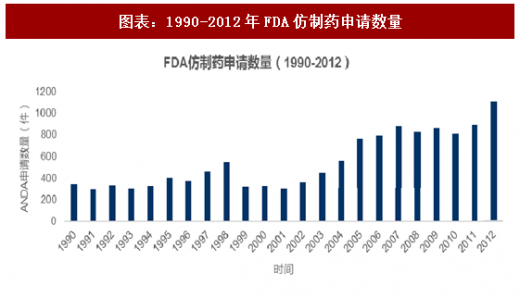
2、把握创新药的衰退期,仿制药企业Teva脱颖而出
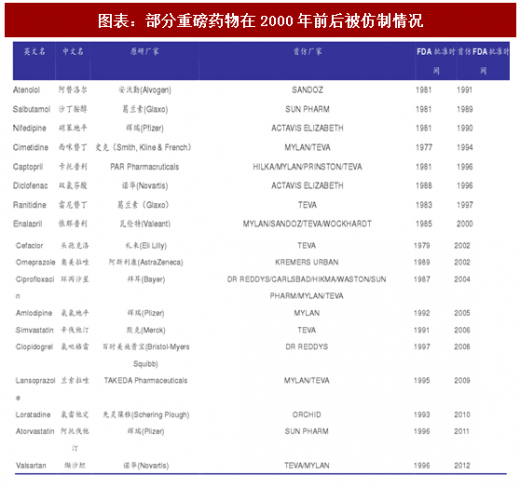
Hatch-Waxman法案提供了有利的政策环境是前提条件,仿制药真正大发展还是在2000年之后,一大批1970-1980年代研发的重磅药物专利纷纷到期,为仿制药物的生产厂家提供了大量的高质量仿制标的。大量重磅药物仿制产品的上市大大降低了患者的治疗成本,扩大了疾病的治疗人群。从1990年起,美国市场上仿制药的处方量稳步提升,在2000年左右已经超过了原研药。从1996-2015的20年间,美国仿制药市场销售额实现了5倍的增长。
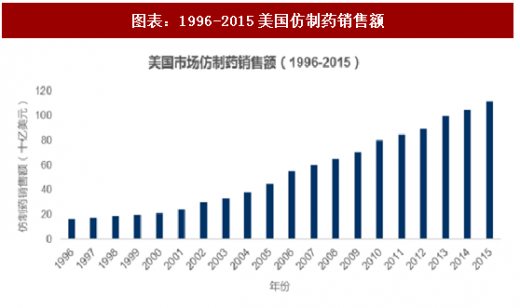

经过近二十年的成长,大量仿制药企业崭露头角,包括以色列的Teva Generics、瑞士公司Sandoz、英国公司Mylan和印度公司DrReddys、Ranbaxy、Sun Pharm等。
我们这里以Teva为例,分析仿制药企业是如何抓住创新药衰退期专利悬崖的机会快速做强做大。
与仿制药行业众多厂家一样,TEVA于1984年Hatch-Waxman法案颁布后进入仿制药行业。1985年,TEVA与W.R.GRACE在美国合资成立TAG Pharmaceuticals,并收购美国仿制药公司Lemmon,正式进军美国仿制药市场。1987年,TEVA在美国NASDAQ上市。
随着2000年后大批重磅药物专利到期,TEVA也迎来了公司发展的黄金时代。2000-2009年间,TEVA共有158个仿制药产品被FDA批准上市,其中包括依那普利、环丙沙星、盐酸舍曲林、辛伐他汀、兰索拉唑等重磅炸弹,且TEVA均取得了这些重磅炸弹的首仿市场独占权,为公司带来了巨大的收益。在1995-2010年期间,TEVA股价上涨了约19倍,可谓风头正劲。2010年之后随着专利过期高峰结束,首仿过后其他仿制药企业参与竞争,2011年至今涨幅仅2%。
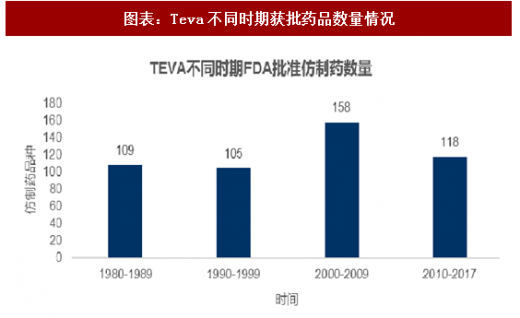
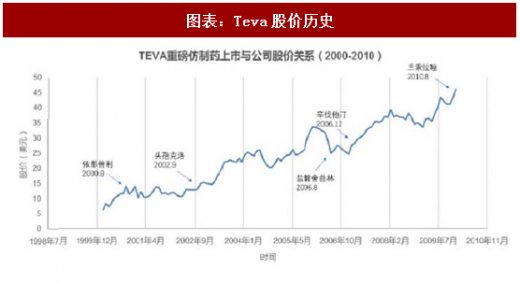
参考观研天下发布《2018年中国创新药行业分析报告-市场深度分析与发展趋势预测》
三、创新药周期理论的应用之三:我国医药工业站在新一轮周期的起点
我们认为国内医药工业处于新一轮创新药周期的山脚。
回顾上一轮以攻克心脑血管疾病、糖尿病为驱动的创新药周期,最获益的无疑是80、90年代日本药企的跟随式创新,以及以色列、印度等国家仿制药企业2000-2010年的利用创新药衰退期产生的专利悬崖进行快速扩张。中国现代医药工业起步于20世纪末期,而此时全球上一轮医药创新周期已经从销售黄金期步入衰退期,国内药企失去了模仿日本创新药的机会,所以国内以仿制药为主,但是仿制药的临床治疗属性不及进口原研药,补贴医院收入属性不及独家大品种。在医保扩容,蛋糕做大的背景下,补贴属性需求压过治疗属性需求,形成了进口药用来解决临床需求,国产独家品种用来补贴医生收入的二元结构,从抗生素到中药注射剂无不例外。我们认为新一轮创新药周期的大幕已经徐徐拉开,此轮周期的核心驱动力是肿瘤从绝症向慢性病的转化,现在正处于研发突破期,创新药将会兼顾治疗属性与补贴属性,相应会产生一批伟大的企业,下文我们将具体展开分析。1、制剂出口?or自主创新?十年之争的终结
自主创新本质上是做进口替代解决国内医疗需求,制剂出口是瞄准全球市场出口创汇。
解决国内医疗需求的药企以恒瑞医药为代表,齐鲁制药、扬子江、天士力、石药集团、正大天晴、步长制药等,多为北方企业,核心竞争力是独家品种+覆盖全中国的销售网络。仿制药出口创汇以华海药业为代表,包括普利制药、海正药业、浙江医药,乃至新和成等,多为浙江企业,可能与浙江沿海地区外贸导向的经济特点有关,核心竞争力是控制成本与质量管控。
2005前后,我国先后涌现了一批以制剂出口突围方向的药企,先行者前有海正药业,后有华海药业、普利制药等;几乎是同时期,2006年申万医药发表了恒瑞医药历史上首篇深度报告《恒瑞医药:自主创新开启公司走向医药贵族之门》,第一次提出恒瑞医药将凭借良好的研发基础在国内众多仿制药企业中脱颖而出,成为A股创新药标杆。
自此“自主创新”与“制剂出口”成为公认的国内药企杀出重围的两条道路,如今十几年过去了,但问路在何方,资本市场似乎已经给出了答案。制剂出口的药企:华海药业接近300亿市值,海正药业130亿市值,普利制药80亿市值,虽然ANDA数量还在不断上升,但似乎市场的投资逻辑已经从出口美国快速放量转换为一致性评价走捷径出口转内销,普利制药主攻的方向也是海外仿制药巨头不重视的注射剂市场;反观自主创新,恒瑞医药市值一度超过2000亿市值,复星医药1000亿市值,康弘药业400亿市值,贝达药业250亿市值。自主创新型药企在市值上形成了对制剂出口药企的全面碾压。如果将视野扩大到其余的大市值医药公司,云南白药、华东医药、信立泰、天士力、步长制药等,也都是以解决国内医疗需求为核心的。
正如我们上一章分析的,以前资本市场觉得我国仿制药与印度仿制药有15年左右的发展差距,如今15年过去了,这种差距仍然较大,不是因为我国仿制药企业自身不够努力,而是因为这15年恰好是创新药专利集中过期的15年,等华海们练好内功抵达美国的时候,Teva们已经把心脑血管大品种的首仿占尽了,错过了最佳窗口期。
从大背景上来说,90年代初冷战结束,美国成为唯一的超级大国,对外为全世界人民研发创新药,对内进一步提高全民医疗福利,具体表现为高医疗投入支持高药价,高药价支撑高医药研发支出,而最终的研发成果被印度等国家免费使用,被中国等国家以2折的价格使用(参考索非布韦美国与中国定价的差异)。这种畸形的模式令美国的医疗支出/GDP从1980年的9%上升到2015年的17%,远高于其他西方发达国家,随着美国国力整体的相对衰弱,我们认为这种美国埋单全世界受益的模式难以为继,美国版本的医保控费正在进行时,主打制剂出口的中国药企面对的是强大的以色列、印度仿制药对手,以及一个正在恶化的美国药品市场。制剂出口还是自主创新解决内需,十年的争论可以结束了,我们认为未来必将属于可以解决国内医疗需求的药企。
2、以攻克癌症为驱动的新一轮创新周期大幕徐徐拉开:为什么是肿瘤?
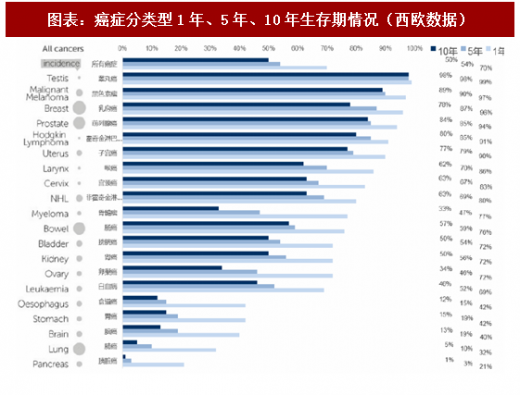
因为人种、饮食习惯等原因,东亚人口与美国人口疾病谱分布存在明显差异。考虑人种、饮食习惯两方面的因素,我们认为可以参考日本、新加坡两地疾病谱分布。2016年我国全国平均预期寿命为76.1岁,《统计年鉴》没有2016年我国分省份的人口预期寿命数据,最新数据更新到2010年,当时我国人口预期寿命为74.8岁,经济较发达地区如北京、上海人口预期寿命分别为80.2岁、80.3岁。我们判断东部沿海经济发达地区人口预期寿命已经与日本、新加坡接近。
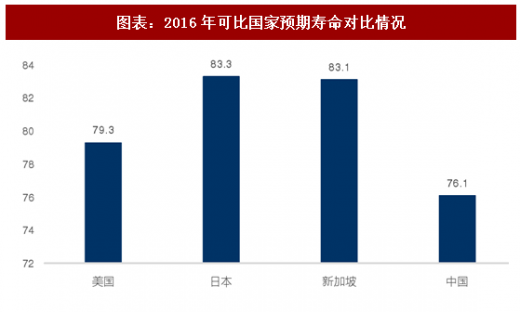
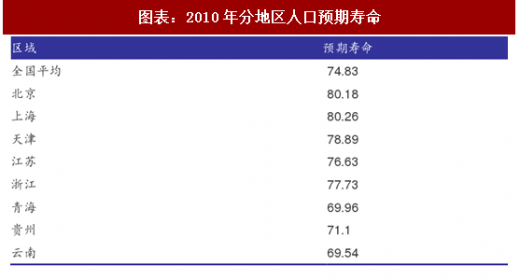
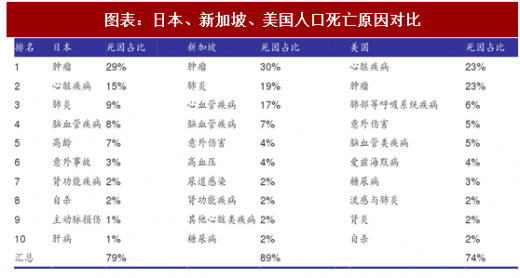
由表格可见,东亚人种与美国人种疾病谱存在差异,无论是日本还是新加坡死亡率排名第一位的疾病都是恶性肿瘤。随着我国人口平均寿命向日本、新加坡靠近,恶性肿瘤发病率有进一步提高的趋势。攻克肿瘤,使之从绝症向慢性病转化是未来10-15年的核心矛盾。
3、本轮以攻克肿瘤为驱动的新周期已经发展到研发突破期
基础技术积累已经完成:2000年以来人类基因组学突飞猛进,对肿瘤的发病机制有了更加深刻的认识,发现了一系列与肿瘤生长相关的基因、蛋白质(酪氨酸激酶、内皮抑素等),基因测序与循证医学得以相互交叉,精准医学的理念逐渐深入人心,这一切都确定了免疫治疗、靶向治疗的理论基础;另一方面CRISPR-CAS9等基因编辑技术为细胞治疗提供了技术实现手段。
肿瘤药的发展自1940年开始经历了三次革命,分别为化疗、靶向药、免疫治疗+细胞治疗。2011年免疫疗法的问世带来了使肿瘤成为慢性病的希望,援引《Science》杂志的评价:“This year marks a turning point in cancer”,使我们确信肿瘤领域的研发突破期已经到来了。
1.1940-1990年代,化疗药物:顺铂、砒霜、多西他赛、紫杉醇等。常用的化疗药物有几十种,机理各有不同,但是无论机理如何,它们作用都是杀死快速分裂的细胞,但是化疗药物的死穴是它们并不能区分恶性细胞还是正常细胞,因此化疗药物在杀死癌细胞的同时,也会杀死大量人体正常分类细胞。
2.2000至今,分子靶向药。由于普通化疗的治疗指数低,副作用强,科学家一直在寻找特异性杀死癌症细胞而不影响正常细胞的治疗手段。70年代致癌基因的发现使这个想法成为了可能,科学家开始尝试开发特异的药物来抑制癌症独有的致癌基因。2001年第一个分子靶向药格列卫(Gleev e c)在2001年横空出世,让BCL-ABL突变基因慢性白血病病人五年存活率从30%一跃到了89%。
3.2011年开始,免疫疗法+细胞治疗。免疫疗法与细胞治疗的原理市场上的报告已经阐述的很详细了,我们重点截取了一些临床数据,证明免疫疗法+细胞治疗让癌症成为慢性病成为可能。
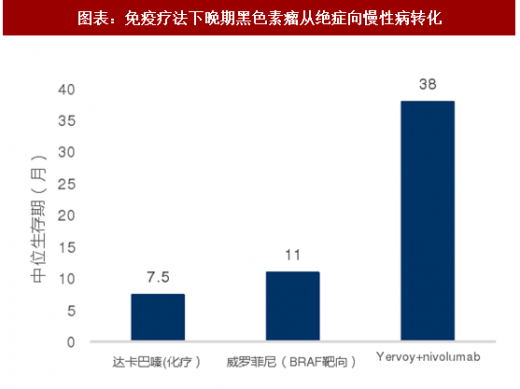
免疫疗法:2011年第一个免疫激活药物Yervoy上市,由于应答率低、副作用强没有太多波澜。2013年同靶点的Opdivo、Keytruda上市发布了令人震惊的临床结果:在所有已有治疗方案都失效的黑色素癌晚期病人这两个药物让60%以上的病人肿瘤减小乃至消失了超过2年。曾经这些晚期转移病人平时的生存时间只能以周计算。以前任何一个有效的化疗或者靶向治疗药物的目标都是延长1~2个月的生存时间,免疫疗法使患者中位生存期从11个月延长至38个月。
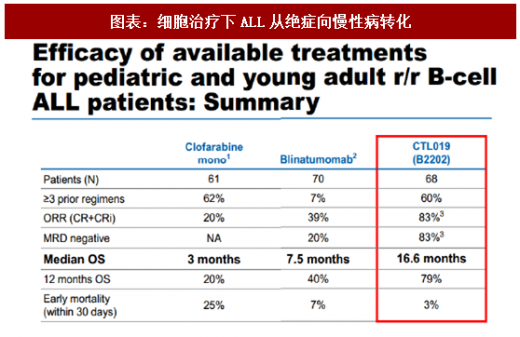
细胞治疗:2010年CarlJune用CAR-T疗法治愈了3个复发、难治型白血病患者后,细胞治疗从科学探索阶段逐步走向临床试验产业化,2017年8月诺华CAR-T正式获批上市。根据已经公开的诺华的CTL019申报材料,复发难治性急性淋巴细胞白血病的缓解率高达83%,远高于化疗疗法氯法拉滨的20%以及Amgen单抗药物Blinatumomab的39%。患者中位生存期从3个月一举提高到16.6个月。
4、肿瘤从绝症到慢性病转换带来的市场扩容测算
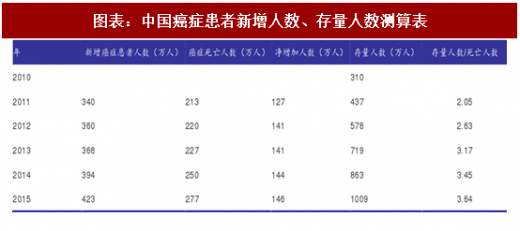
根据中国癌症中心公布的我国癌症发病率、死亡率数据,我们对癌症存量患者人数进行了测算,估算2017年存量肿瘤患者接近1300万人。我们用存量患者/死亡人数,粗略测算患者生存时间,结合新发病人数估算,患者中位生存时间在3年左右。
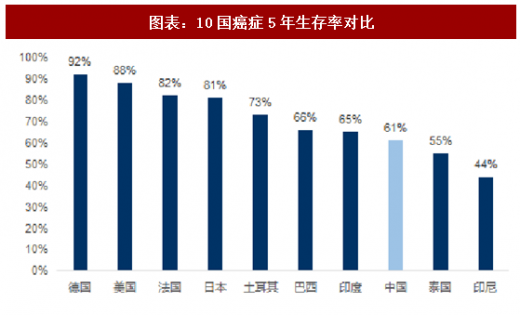
美国、德国、日本癌症患者生存期超过5年,一旦肺癌、肝癌等5年存活率较低的疾病被攻克,癌症生存期有望从5年向8年迈进。带癌生存期的增加带来的是存量患者的扩容,我国目前每年新增肿瘤患者400万人左右,目前生存中位数是3年左右,存量患者人数1300万人。若癌症完成从绝症到慢性病的转换,生存期从3年延长至8年,则存量患者人数将达到3200万人以上,会出现销售额在几百亿人民币的肿瘤大品种。
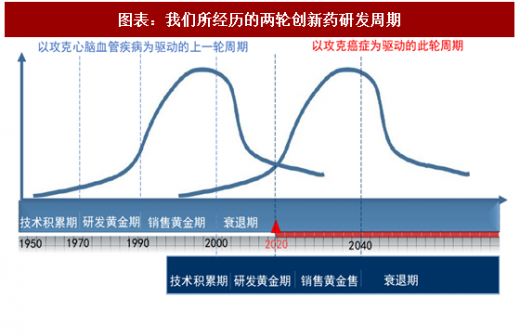
我们判断我们正处于新一轮创新药周期的第二阶段,把握这段投资机会,就要复制日本在80年代、90年代的跟随式创新。未来在医保控费的形势下,最为得利的是既能满足临床需求又能兼顾补贴医疗机构收入需求的国产品种。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。